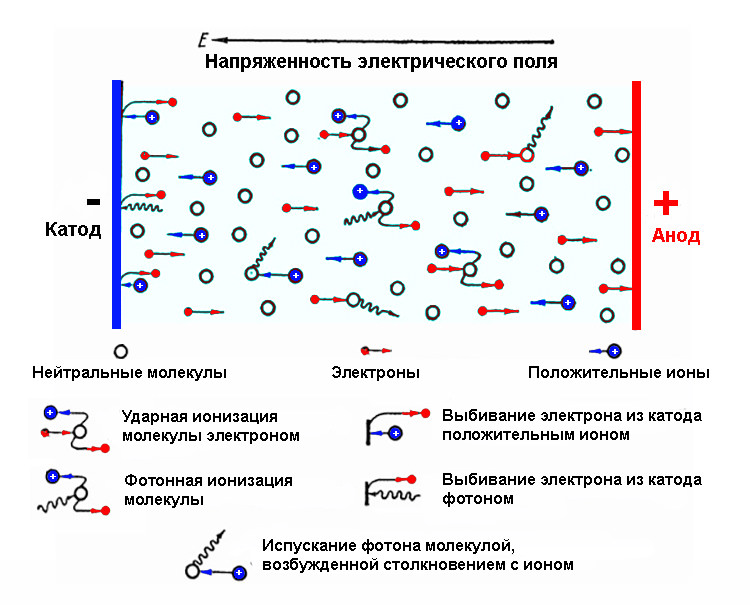
Будова електронних оболонок атома
Коротко згадаємо, як влаштована електронна структура атома. Вона складається з оболонок, що позначаються літерами K, L, M, N, O, P, Q або цифрами від 1 до 7. Електрони в межах оболонки характеризуються однаковим головним квантовим числом n, що визначає можливі значення енергії. У зовнішніх оболонках енергія електронів вище, а потенціал іонізації для зовнішніх електронів відповідно нижче.
Оболонка включає один або декілька підрівнів: s, p, d, f, g, h, i. У кожній оболонці кількість підрівнів збільшується на один порівняно з попередньою. Кількість електронів у кожному підрівні і в кожній оболонці не може перевищувати певного значення. Вони характеризуються, крім головного квантового числа, однаковим значенням орбітального квантового числа, визначає форму електронної хмари. Підрівні позначаються із зазначенням оболонки, якій вони належать, наприклад, 2s, 4d і так далі.
Підрівень містить атомні орбіталі, які задаються, крім головного і орбітального, ще одним квантовим числом – магнітним, що визначає проекцію орбітального моменту електрона на напрямок магнітного поля. Одна орбіталь може мати не більше двох електронів, що розрізняються значенням четвертого квантового числа – спінової.
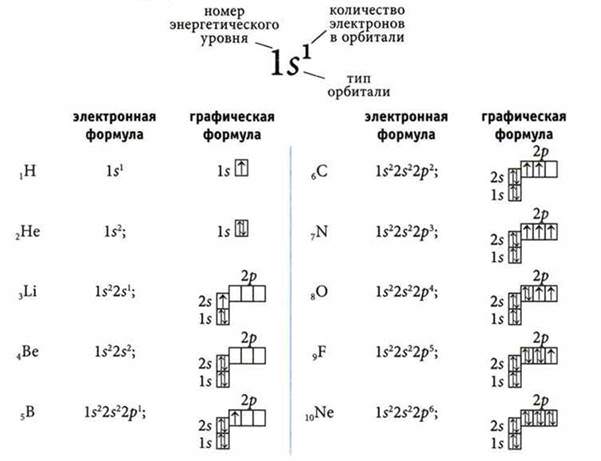
Розглянемо докладніше, як виникає характеристичне рентгенівське випромінювання. Так як походження цього типу електромагнітної емісії пов’язане з явищами, що відбуваються всередині атома, зручніше всього описувати його саме в наближенні електронних конфігурацій.