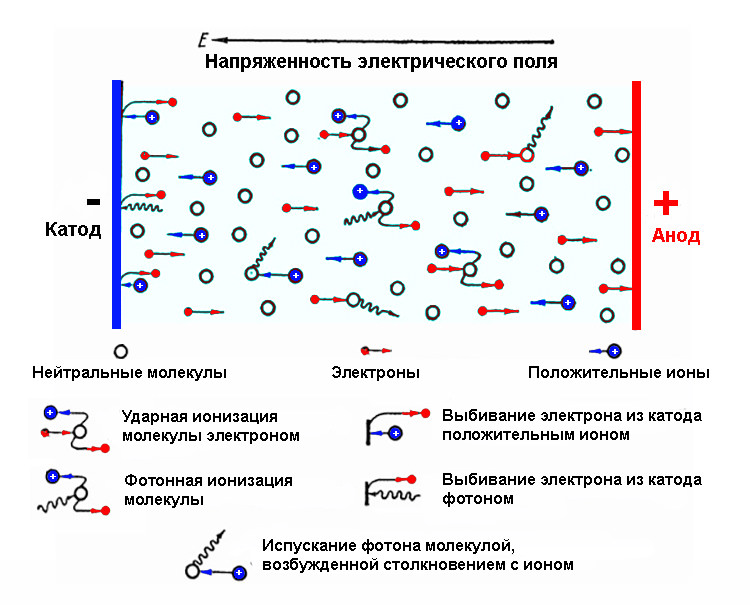
Золото – вкрай малоактивний метал. Навіть у природі воно зустрічається, в основному, у вигляді самородків (на відміну від лужних і лужноземельних металів, що перебувають виключно у складі мінералів або інших сполук). При довгому знаходженні на повітрі воно не окислюється киснем ( цей благородний метал цінують в тому числі і за це). Тому знайти, ніж розчиняється золото, досить складно, але можна.
Промисловий метод
При видобутку золота з так званих золотоносних пісків доводиться працювати з суспензією приблизно однаково дрібних частинок золота і піщинок, які потрібно відокремити один від одного. Можна зробити це з допомогою промивання, а можна використовувати ціанід натрію або калію – різниці немає. Справа в тому, що золото утворює розчинну комплекс з ціанід-іонами, а пісок не розчиняється і залишається як є.

Ключовим моментом у цій реакції є наявність кисню (того, що міститься в повітрі, досить): кисень окисляє золото в присутності ціанід-іонів і виходить комплекс. При недостатній кількості повітря або сама по собі без ціаніду реакція не йде.
Зараз це найбільш поширений спосіб промислового одержання золота. Звичайно, до отримання кінцевого продукту ще багато стадій, але нас цікавить конкретно цей етап: розчини ціанідів – те, що розчиняється золото.
Амальгама
Процес амальгамації також застосовують у промисловості, тільки вже при роботі з рудами і твердими породами. Суть його полягає у здатності ртуті утворювати амальгаму – інтерметалічна сполука. Строго кажучи, ртуть в цьому процесі не розчиняє золото: воно залишається в амальгамі в твердому вигляді.
При амальгамації йде змочування породи рідкою ртуттю. Однак процес “витягування” золота у амальгаму довгий, небезпечний (пари ртуті отруйні) і малоефективний, тому цей метод вже рідко де застосовують.
Царська горілка
Є багато кислот, здатних роз’їдати живі тканини і залишати страшні хімічні опіки (аж до летального результату). Однак немає такої одиночної кислоти, в якій розчиняється золото. З усіх кислот подіяти на нього може тільки знаменита суміш – царська горілка. Це азотна і соляна (хлороводородная) кислоти, взяті в співвідношенні 3 до 1 за об’ємом. Чудові властивості цього пекельного коктейлю обумовлені тим, що кислоти беруться у дуже великих концентраціях, що сильно підвищує їх окислювальну здатність.
Царська горілка починає діяти з того, що азотна кислота починає окислювати спершу соляну, і в ході цієї реакції утворюється атомарний хлор – дуже реакционноспособная частинка. Саме вона йде на атаку золота і утворює з ним комплекс – золотохлорістоводородную кислоту.

Це дуже корисний реактив. Дуже часто золото зберігають в лабораторії саме у вигляді кристалогідрату такий кислоти. Нам воно служить лише підтвердженням того, що золото розчиняється в царській горілці.

Варто ще раз звернути увагу на те, що окисляє метал у цій реакції не одна з двох кислот, а продукт їх взаємної реакції. Так що якщо взяти, наприклад, одну лише “азотку” – відому кислоту-окислювач – нічого не вийде. Ні концентрація, ні температура не зможуть зробити так, щоб золото розчинилося в азотній кислоті.
Хлорка
На відміну від кислот, зокрема соляної кислоти, окремі речовини можуть стати тим, чим розчиняється золото. Широко відома побутова хлорка – розчин газоподібного хлору у воді. Звичайно, звичайним магазинним розчином нічого не зробиш, потрібні концентрації вище.
Хлорна вода діє наступним чином: хлор дисоціює на соляну і на хлорнуватисту кислоти. Хлорнуватиста кислота під світлом розкладається на кисень і соляну кислоту. У такому розкладанні виділяється атомарний кисень: як і атомарний хлор в реакції з царською горілкою, він дуже активний і окислює золото за милу душу. У підсумку знову виходить комплекс золота з хлором, як і в попередньому способі.

Інші галогени
Крім хлору, золото також непогано окислюють та інші елементи сьомої групи таблиці Менделєєва. В повній мірі сказати про них: “те, у чому розчиняється золото” – важко.
З фтором золото може реагувати по-різному: при прямому синтезі (з температурою 300-400°С) утворюється фторид золота III, який у воді негайно гідролізується. Він настільки нестійкий, що розкладається навіть при впливі плавикової (фтороводородной) кислоти, хоча серед фторид-іонів йому повинно бути комфортно.
Також дією сильних окислювачів: фторидів благородних газів (криптону, ксенону) можна отримати і фторид золота V. Такий фторид взагалі вибухає при контакті з водою.
З бромом справи йдуть трохи простіше. Бром в звичайних умовах – рідина, і золото непогано розсіюється в його розчинах, утворюючи розчинний бромід золота III.
З йодом золото також реагує при нагріванні (до 400°С), утворюючи йодид золота I (така ступінь окислення пояснюється меншою активністю йоду порівняно з іншими галогенами).
Таким чином, золото, безсумнівно, реагує з галогенами, проте розчиняється чи золото в них – спірне твердження.
Розчин Люголя
Насправді, йод (звичайний йод I2) у воді не розчиняється. А розчинний його комплекс з йодидом калію. Це з’єднання називається розчином Люголя – і він вміє розчиняти золото. Між іншим, їм же часто змащують горло хворіють на ангіну, так що не все так однозначно.
Ця реакція також йде через утворення комплексів. Золото утворює з йодом комплексні аніони. Використовується, як правило, для травлення золота – процес, при якому взаємодія йде тільки з поверхнею металу. Розчин Люголя зручний у цьому випадку, тому що на відміну від царської горілки і ціанідів, реакція йде помітно повільніше (і реактиви доступнішим).
Бонус
Говорячи про те, що поодинокі кислоти – це те, в чому золото не розчиняється, ми трохи збрехали – насправді такі кислоти є.
Хлорне кислота – одна з найсильніших кислот. Її окислювальні властивості надзвичайно високі. В розбавленому розчині вони виявляються погано, проте у великих концентраціях творять чудеса. При реакції утворюється її сіль перхлорат золота – жовтий і нестійкий.
З кислот, в яких розчиняється золото, є ще гаряча концентрована селеновая кислота. В результаті також утворюється сіль – селенат золота червоно-жовтого кольору.