Закони хімічної термодинаміки
Перш ніж розглядати основні постулати, необхідно згадати суть величин, що характеризують стан різних систем.
Під внутрішньою енергією системи U розуміють запас її енергії, що складається з енергій руху і взаємодії частинок, тобто всіх видів енергії за винятком кінетичної енергії та її потенційної енергії положення. Визначити її зміна ∆U.
Ентальпію Н часто називають енергією розширеної системи, а також її теплосодержанием. H=U+pV.

Теплотою Q називають неупорядковану форму передачі енергії. Внутрішня теплота системи вважається позитивною (Q > 0), якщо тепло поглинається (ендотермічний процес). Негативна (Q < 0) вона в тому випадку, якщо тепло виділяється (екзотермічний процес).
Роботою А називають упорядковану форму передачі енергії. Вона вважається позитивною (A>0), якщо здійснюється системою проти зовнішніх сил, і негативною (A<0), якщо здійснюється зовнішніми силами над системою.
Основним постулатом є перший початок термодинаміки. Існує безліч його формулювань, серед яких можна виділити наступну: “Перехід енергії з одного виду в інший відбувається в строго еквівалентних кількостях”.
Якщо система здійснює перехід із стану 1 в стан 2, супроводжується поглинанням теплоти Q, яка, в свою чергу, витрачається на зміну внутрішньої енергії ∆U і здійснення роботи А, то математично цей постулат записується рівнянням: Q=∆U+A, або δQ = dU + δA.
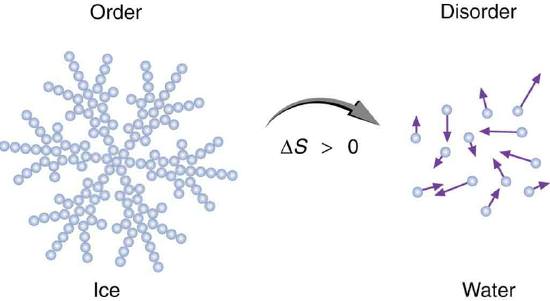
Другий закон термодинаміки, як і перший, не виведений теоретично, а носить статус постулату. Однак його достовірність підтверджують слідства з нього відповідні експериментальним спостереженням. У фізичній хімії частіше зустрічається наступна формулювання: “У будь-якої ізольованої системи, яка не перебуває у стані рівноваги, ентропія зростає з плином часу, причому триває її зростання, поки система не увійде в стан рівноваги”.
Математично цей постулат хімічної термодинаміки має вигляд: dSизол≥0. Знак нерівності в даному випадку вказує на неравновесность стану, а знак “=” на рівновагу.