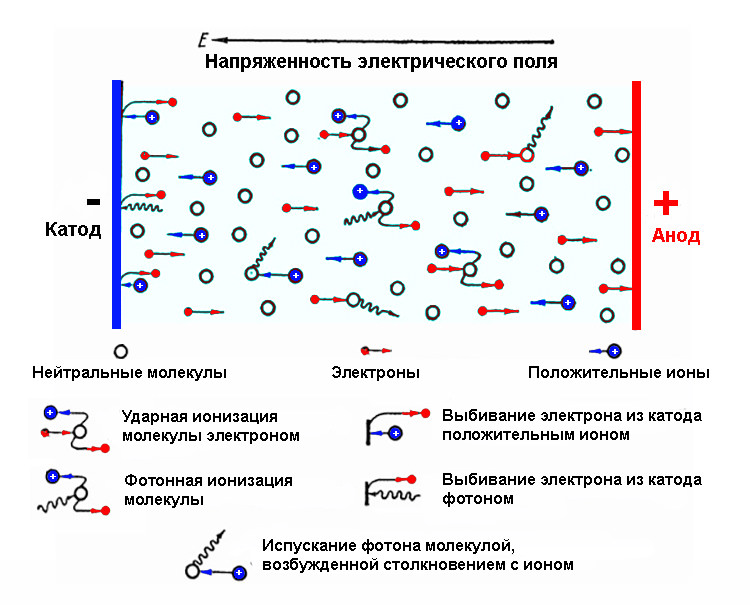
Рівноважні та нерівноважні процеси
У системі основних понять хімічної термодинаміки особливе місце займає термодинамічний процес. Його визначають як зміни в стані системи, які характеризуються змінами одного або декількох термодинамічних параметрів.
Зміни в стані системи можливі при різних умовах. У зв’язку з цим розрізняють рівноважні та нерівноважні процеси. Рівноважний (або квазистатический) процес розглядається як ряд рівноважних станів якої-небудь системи. При цьому всі параметри її змінюються нескінченно повільно. Для протікання такого процесу необхідно дотримання ряду умов:
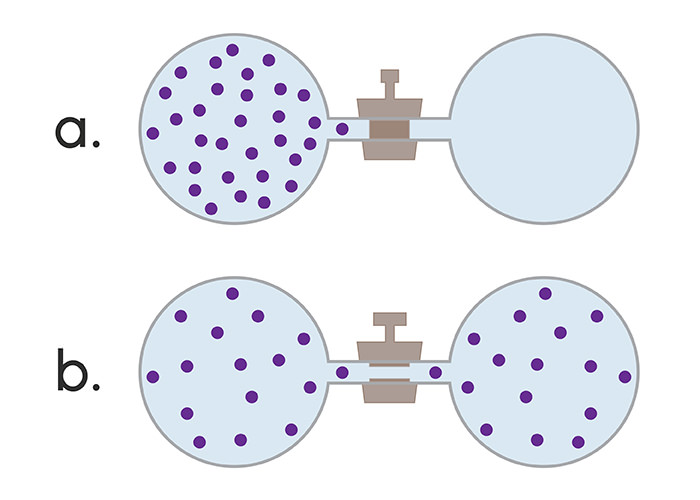
Процес зміни нерівноважного стану системи на рівноважний називають релаксацією, а тривалість його – часом релаксації. У хімічній термодинаміці найчастіше приймають найбільше значення часу релаксації для якого-небудь процесу. Пов’язано це з тим, що реальні системи легко виходять із стану рівноваги виникають потоками енергії та/або речовини в системі і є нерівноважними.