Концентрація
Розглянемо основні фактори, що впливають на швидкість реакції. Почнемо з концентрації. Подібна залежність виражається законом діючих мас. Між твором концентрацій речовин, що вступають у взаємодію, взятих в ступені їх стереохимических коефіцієнтів, і швидкістю протікання реакції, існує прямо пропорційна залежність.
Розглянемо рівняння аА +вв = сС + дД, де А, В, С, Д – є рідинами або газами. Для наведеного процесу кінетичне рівняння можна записати з урахуванням коефіцієнта пропорційності, який для кожного взаємодії має своє значення.
В якості основної причини зростання швидкості можна відзначити збільшення кількості зіткнень реагуючих частинок в одиниці об’єму.
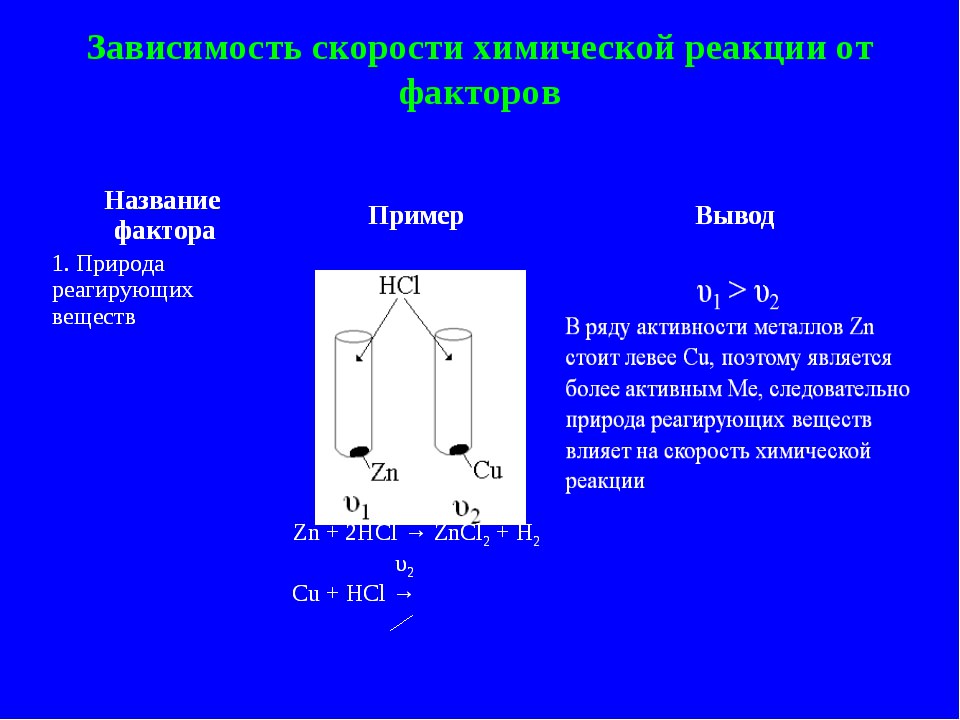
Температура
Розглянемо вплив температури на швидкість реакції. Процеси, які протікають в гомогенних системах, можливі тільки при зіткненні частинок. Але далеко не всі зіткнення призводять до утворення продуктів реакції. Тільки в тому випадку, коли у частинок є підвищена енергія. При нагріванні реагентів спостерігається збільшення кінетичної енергії часток, зростає кількість активних молекул, тому спостерігається підвищення швидкості реакції. Зв’язок між температурним показником і швидкістю процесу визначається правилом Вант-Гоффа: кожне збільшення температури на 10°С призводить до зростання швидкості процесу в 2-4 рази.