Механізми реакції
В літературі описують два можливі шляхи протікання реакції, і обидва вони проходять за принципом електрофільного заміщення. Різниця полягає лише в природі електрофени: у першому випадку це алкильный карбониевый іон (інша назва – карбокатион), що утворюється в результаті приєднання галоген-іона до кислоти Льюїса за донорно-акцепторної принципом, а в другому – одностадійне створення внутрішнього комплексу між усіма учасниками реагентами за тим же способом. Нижче детально розглянуто кожен з можливих варіантів.
Реакція з утворенням іона карбониевого
Даний механізм передбачає проходження синтезу в 3 стадії, де кислоти Льюїса, наприклад, AlCl3, TiCl4, SnCl4, FeCl3, BF3, HF виступають у якості каталізатора процесу.
Для розгляду типової реакції Фріделя-Крафтса було обрано взаємодія між бензолом і 1-фторпропаном (C3H6F) в присутності трифтористого бору BF3 як каталізатора.
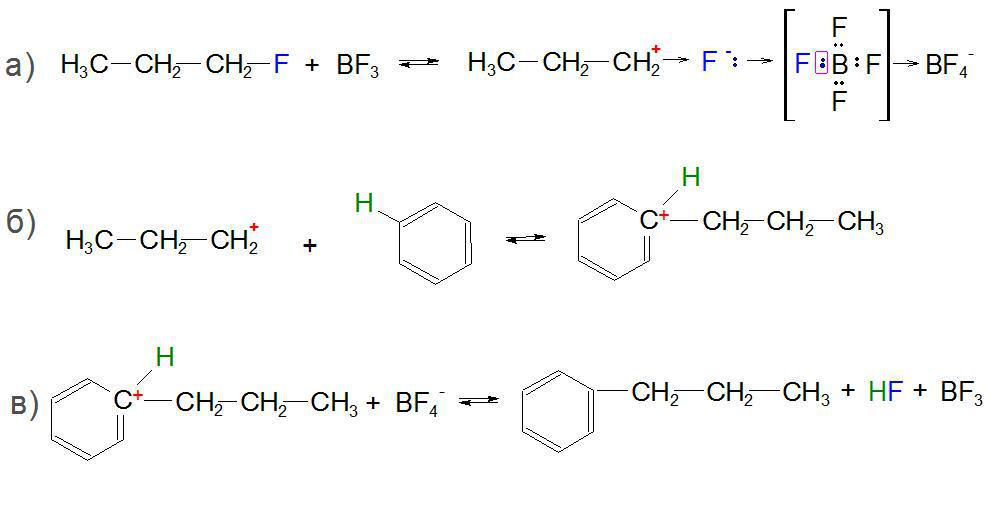
У першій стадії процесу C3H6‒F реагує з BF3, приєднуючи галоген-іон за донорно-акцепторної принципом. На зовнішньому енергетичному рівні у бору є вільна комірка (акцептор), яку займає фтор з неподіленої парою електронів (донор). Завдяки такому приєднання атом вуглецю C, що стоїть поруч з галогеном F в 1-фторпропане, здобуває позитивний заряд і стає дуже реакционноспособным пропіл-карбониевым іоном. Це властивість даних іонів збільшується в ряду первинний→ вторинний→ третинний, тому в залежності від умов в продуктах реакції алкілування можлива перегрупування бічного ланцюга у більш вигідне становище.
Далі, отриманий карбокатион реагує з бензолом і приєднується в місці зв’язку атомів вуглецю і водню, передаючи електронну щільність на C ароматичного кільця.
У третій стадії новоутворена частка реагує з іонізованою кислотою Льюїса, де атом H відщеплюється від арена і приєднується до ісмаелю, який відірвався F з утворенням фтороводень HF, а продуктами реакції стає н-пропилбензол, изопропилбензол і відновлений BF3.